《硫酸》高一必修二PPT课件(第5.1.2课时).pptx


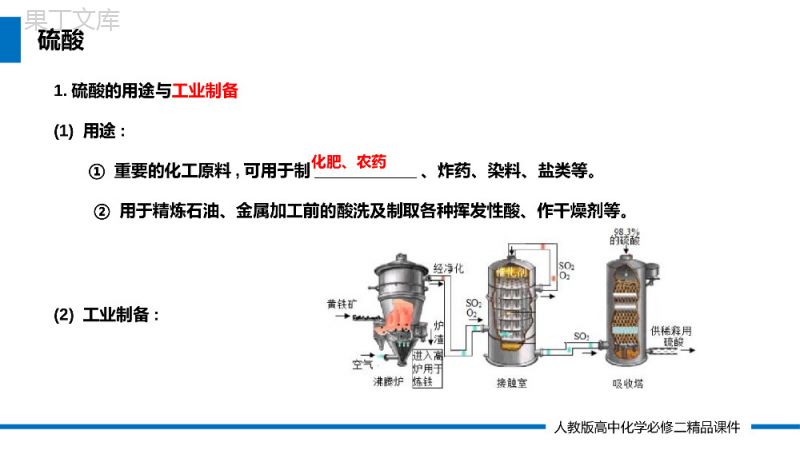
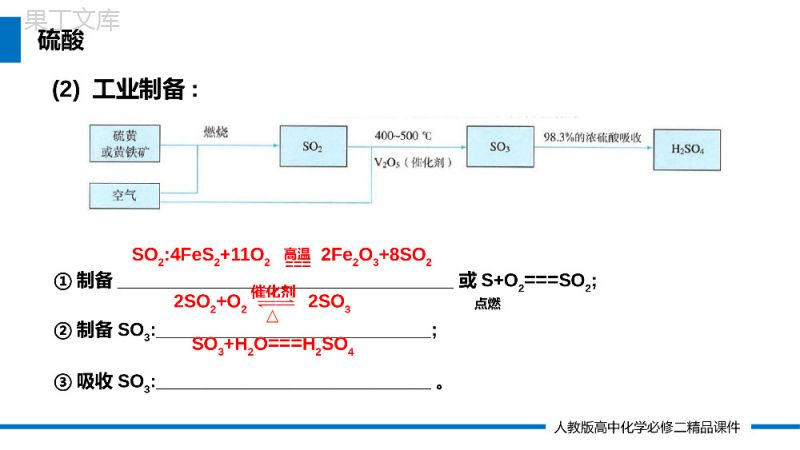
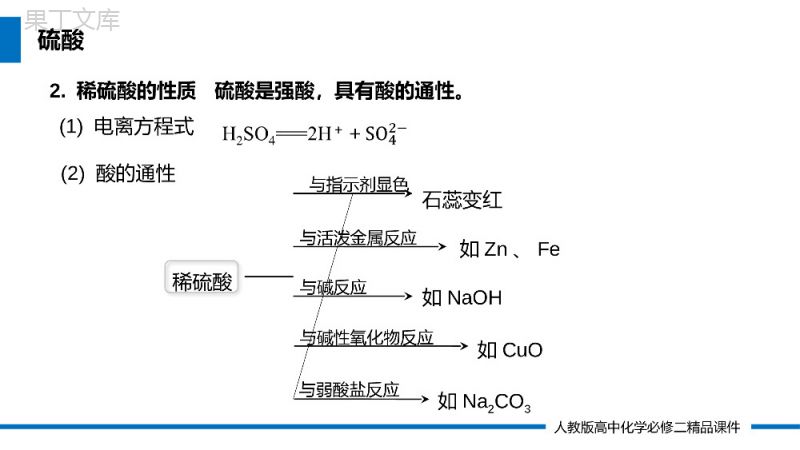
人教版化学必修二第一节硫及其化合物第五章化工生产中的重要非金属元素PleaseEnterYourDetailedTextHere,TheContentShouldBeConciseAndClear,ConciseAndConciseDoNotNeedTooMuchText第2课时硫酸主讲人:办公资源时间:20XX.4.4LOGO人教版高中化学必修二精品课件学习目标与核心素养学习目标1、了解浓硫酸的三大特性。2、能运用氧化还原反应知识理解浓硫酸的氧化性。3、认识硫酸在相关反应中体现的性质。核心素养1、通过对浓硫酸性质的学习,培养学生论据推理与模型认知的化学核心素养。2、通过对化学实验的设计及操作的学习,培养学生科学探究与创新意识的化学核心素养。人教版高中化学必修二精品课件1.硫酸的用途与工业制备(1)用途:①重要的化工原料,可用于制___________、炸药、染料、盐类等。②用于精炼石油、金属加工前的酸洗及制取各种挥发性酸、作干燥剂等。化肥、农药(2)工业制备:硫酸人教版高中化学必修二精品课件(2)工业制备:①制备_________________________________或S+O2===SO2;②制备SO3:___________________________;③吸收SO3:___________________________。SO2:4FeS2+11O22Fe2O3+8SO22SO2+O22SO3SO3+H2O===H2SO4高温点燃△催化剂===硫酸人教版高中化学必修二精品课件2.稀硫酸的性质硫酸是强酸,具有酸的通性。(2)酸的通性与指示剂显色石蕊变红与活泼金属反应如Zn、Fe与碱反应如NaOH与碱性氧化物反应如CuO与弱酸盐反应如Na2CO3(1)电离方程式稀硫酸硫酸人教版高中化学必修二精品课件1、写出下列反应的离子方程式:(1)稀硫酸与活泼金属反应,如Zn:______________________。(2)稀硫酸与金属氧化物反应,如CuO:______________________。(3)稀硫酸与碱反应,如NaOH:____________________________。(4)稀硫酸与部分盐反应,如Na2CO3:_______________________。Zn+2H+===Zn2++H2↑CuO+2H+===Cu2++H2OOH-+H+===H2O+2H+===CO2↑+H2O23CO课堂练习23CO人教版高中化学必修二精品课件3.浓硫酸的特性(1)吸水性:浓硫酸能吸收存在于周围环境中的水分,常用做干燥剂(2)脱水性:浓硫酸能将有机物中的氧、氢元素按水的组成比脱去C12H22O11浓硫酸12C+11H2O(蔗糖)硫酸人教版高中化学必修二精品课件3.浓硫酸的特性吸水性与脱水性硫酸人教版高中化学必修二精品课件吸水性脱水性原理浓硫酸能够吸收______________________及固体中的结晶水浓硫酸能把有机物中________________________脱去,剩余黑色的炭区别__________________________________________________应用_________气体、液体中的水分子氢、氧元素按水的组成比物质中含有H2O物质中不含有H2O,只含有氢元素和氧元素作干燥剂3.浓硫酸的特性吸水性与脱水性硫酸人教版高中化学必修二精品课件1、浓硫酸能使蓝色胆矾变为白色,该过程体现了浓硫酸的脱水性还是吸水性?思考交流人教版高中化学必修二精品课件3.浓硫酸的特性①与金属的反应(3)强氧化性硫酸人教版高中化学必修二精品课件3.浓硫酸的特性①与金属的反应(3)强氧化性d将a试管里的溶液慢慢倒入水中,溶液变为_____a试管中铜丝表面__________________________b试管中的品红溶液逐渐变为________c试管中的紫色石蕊溶液逐渐变为________逐渐变黑色,有气泡产生无色红色蓝色Cu+2H2SO4(浓)===CuSO4+SO2↑+2H2O∆硫酸人教版高中化学必修二精品课件Cu+2H2SO4(浓)===CuSO4+SO2↑+2H2O∆问题:(1)该方程式中,谁是氧化剂,谁是还原剂?(超链接)(2)浓硫酸在这个反应中体现了什么性质?(3)实验室用金属和酸反应制取氢气时,往往用稀硫酸、而不用浓硫酸,这是为什么?Cu+2H2SO4(浓)===CuSO4+SO2↑+2H2O氧化性和酸性硫酸盐和SO2思考与交流人教版高中化学必修二精品课件2、浓硫酸能和金属反应,为什么可用铝罐车和铁罐车来运输浓硫酸?常温下,浓硫酸让Fe、Al的钝化思考交流人教版高中化学必修二精品课件a.反应需要加热S+2H2SO4(浓)===3SO2↑+2H2O∆②与非金属反应:b.还原产物一般是SO23.浓硫酸的特性(3)强氧化性C+2H2SO4(浓)===CO2↑+2SO2↑+2H2O∆③与具有还原性的化合物反应,如H2S、HI、HBr、FeCl2等硫酸人教版高中化学必修二精品课件3.浓硫酸的特性(3)强氧化性硫酸人教版高中化学必修二精品课件1、浓硫酸具有A.强酸性,B.强氧化性,C.高沸点、难挥发性,D.脱水性,E.吸水性等性质。以下过程主要表现了浓硫酸的哪些性质?请将答案的字母分别填入括号中。(1)用NaCl固体和浓硫酸在加热条件下制氯化氢气体()(2)用磷矿物[主要成分是Ca3(PO4)2]和硫酸反应制磷酸()(3)浓硫酸干燥H2、O2、Cl2、HCl和SO2等气体()(4)常温下可以用铁或铝的容器贮存浓硫酸()(5)胆矾放在盛浓硫酸的干燥器中变成白色粉末()(6)不能用浓硫酸干燥HBr、HI和H2S等气体()(7)浓硫酸使湿润的蓝色石蕊试纸先变红后变黑()CAEBEBAD课堂练习人教版高中化学必修二精品课件2.实验证明铜在低温下不能和氧气发生反应,也不能和稀硫酸共热发生反应,但工业上却是将废铜屑倒入热的稀硫酸中并不断地通入空气来制取硫酸铜溶液的。铜屑在此状态下发生的一系列化学反应的方程式为____________________________________________。利用铜和浓硫酸在加热条件下也能制备硫酸铜溶液,其化学方程式为____________________________________。以上两种方法哪种好?______________,原因是____________________________________________________________________________________________________________________第一种方法好①制得相同质量的产品,第一种方法消耗的硫酸少,②第二种方法生成SO2,会造成大气污染,③第一种方法节约能源课堂练习感谢您下载68素材平台上提供的PPT作品,为了您和68素材以及原创作者的利益,请勿复制、传播、销售;素材均来源于网络用户分享,故68素材不具备充分的监控能力来审查图片是否存在侵权等情节。68素材不拥有此类图片的版权,本站所有资源仅供学习与交流,不得用于任何商业用途的范围,用户应自觉遵守著作权法及其他相关法律的规定,不得侵犯本网站及权利人的合法权利,给68素材和任何第三方造成损失的,侵权用户应负全部责任。版权声明人教版高中化学必修二精品课件人教版化学必修二感谢各位的仔细聆听第五章化工生产中的重要非金属元素PleaseEnterYourDetailedTextHere,TheContentShouldBeConciseAndClear,ConciseAndConciseDoNotNeedTooMuchText第2课时硫酸主讲人:办公资源时间:20XX.4.4LOGO
提供《硫酸》高一必修二PPT课件(第5.1.2课时).pptx会员下载,编号:1701021067,格式为 xlsx,文件大小为20页,请使用软件:wps,office Excel 进行编辑,PPT模板中文字,图片,动画效果均可修改,PPT模板下载后图片无水印,更多精品PPT素材下载尽在某某PPT网。所有作品均是用户自行上传分享并拥有版权或使用权,仅供网友学习交流,未经上传用户书面授权,请勿作他用。若您的权利被侵害,请联系963098962@qq.com进行删除处理。

 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载 下载
下载